Vers un nouvel outil de diagnostic précoce de la maladie de Parkinson
Détecter les agrégats de protéines, à l’origine de nombreuses pathologies neurodégénératives, permet de combattre ces maladies. Des scientifiques de l'Institut Européen des membranes et de l’Institut des neurosciences de Montpellier (CNRS/Université de Montpellier) proposent une nouvelle méthode, basée sur l’utilisation de nanopores, qui permet une détection semi-quantitative rapide d’agrégats d’α-synucléine, biomarqueurs de la maladie de Parkinson. Ces résultats sont à retrouver dans la revue ACS Central Science.
Les agrégats de protéines sont à l’origine de nombreuses pathologies liées à l’âge. Parmi ces agrégats, l'a- synucléine est un biomarqueur des troubles neurodégénératifs liés la maladie de Parkinson. Le détecter à un stade précoce, bien avant l’apparition des premiers symptômes, est un enjeu majeur pour lutter contre cette maladie. Mais leurs faibles concentrations ainsi que l’état transitoire et le polymorphisme des agrégats rendent leur détection extrêmement difficile.
La stratégie la plus aboutie actuellement, appelée RT-QuIC, repose sur l’amplification des agrégats de protéines préexistants. Elle s’effectue s’effectue par ajout de thiofalivine T, marqueur fluorescent des fibres qui constituent les agrégats, qui requiert plusieurs jours d’incubation avant de pouvoir réaliser la mesure. Outre le temps qu’elle nécessite, cette méthode difficile à mettre en œuvre ne permet pas d’obtenir d’information quantitative sur la concentration et la morphologie des agrégats d’a- synucléine.
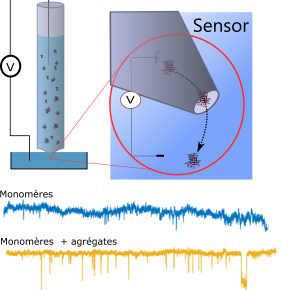
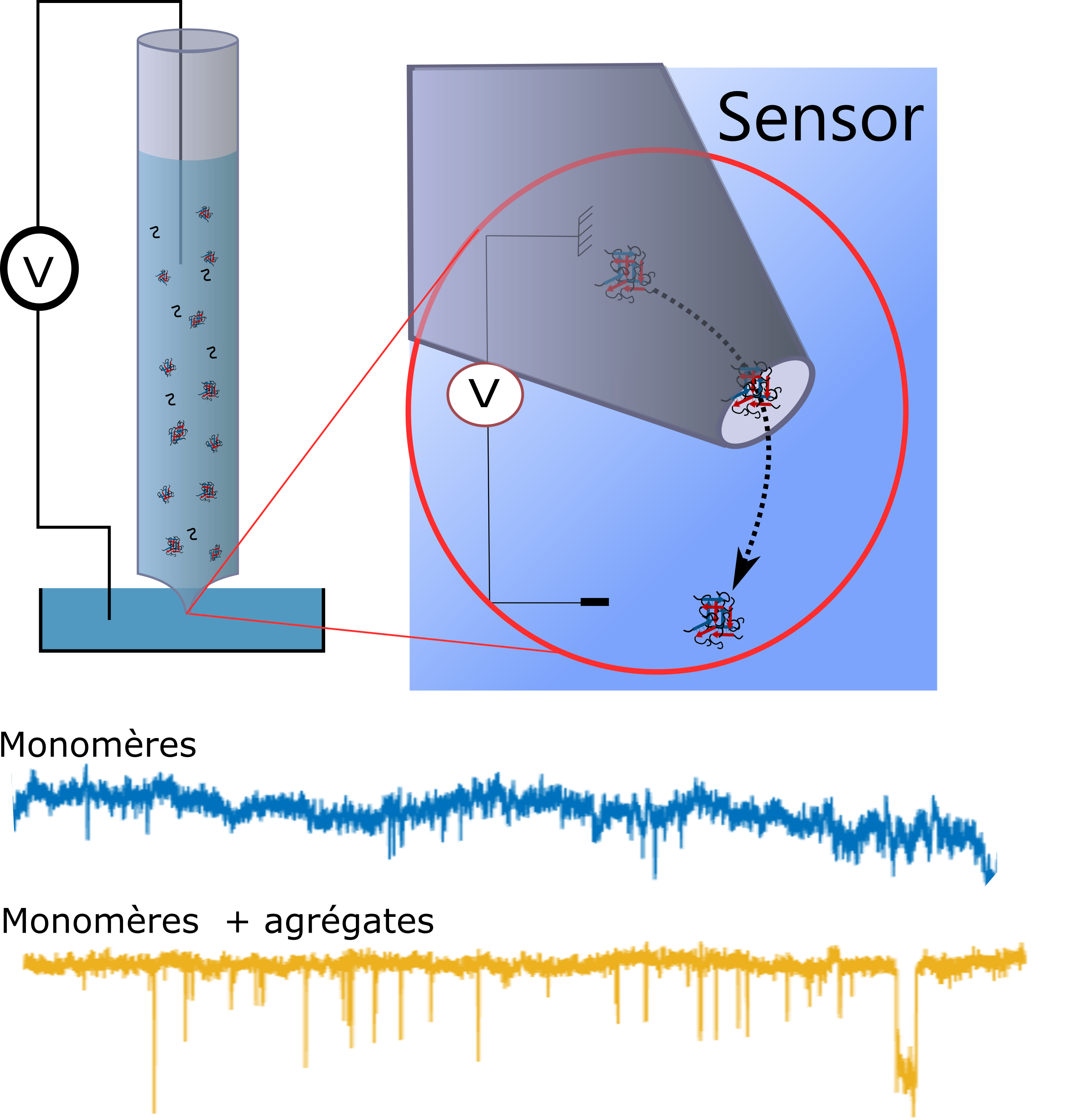
Dans ce contexte, des scientifiques de l'Institut Européen des membranes (CNRS/Université de Montpellier) et de l’Institut des neurosciences de Montpellier (Inserm/Université de Montpellier) ont adapté à la détection des agrégats protéiques à l’origine des troubles neurogénédératifs une méthode dédiée au séquençage de l’ADN utilisant une technologie à base de nanopores, Elle consiste à immerger un pore de taille nanométrique dans une solution d’électrolyte et de mesurer le courant ionique à un voltage constant. La perturbation sur le courant induite par le passage des agrégats dans le nanopore peut alors être corrélée à ses propriétés. Pour cela, ils ont développé un dispositif original utilisant des nanopipette qui permet d’accélérer l’agrégation de l'a- synucléine à partir des agrégats préexistants et de les détecter simultanée en temps réel.
Cette nouvelle méthode baptisée RT-FAST (real-time fast amyloid seeding and translocation) réduit à 90 min le temps nécessaire à l’identification des agrégats d'a- synucléine. Mais mieux encore, elle permet d’obtenir une information sur la concentration des agrégats préformés et permettait, dans le futur, d’accéder à leur taille et leur morphologie, paramètres qui pourraient s’avérer pertinents pour le développement d’outils de diagnostic précoce de la maladie de Parkinson.
Rédacteur : CCdM
Référence
Nathan Meyer, Jean-Marc Janot, Joan Torrent & Sébastien Balme
Real-Time Fast Amyloid Seeding and Translocation of α‑Synuclein with a Nanopipette
ACS Central Science 2022