Un biomatériau innovant pour réactiver l’immunité contre le cancer
L’hypoxie, ou manque local d’oxygène, qui se développe dans les tumeurs cancéreuses agressives est un des principaux obstacles à l’efficacité des immunothérapies. Elle altère profondément la fonction des cellules immunitaires tout en favorisant la survie des cellules cancéreuses. Des scientifiques sont parvenus à contrer ce phénomène en développant un biomatériau innovant capable d’acheminer de l’oxygène au sein de la tumeur et y restaurer l’activité antitumorale des cellules immunitaires. Ces résultats, parus dans la revue Cell Biomaterials, ouvrent de nouvelles perspectives en oncologie.
Pour de nombreux cancers qui se développent par croissance de tumeurs solides, l’hypoxie, ou manque d’oxygène dans les tissus, est un frein majeur à l’action des cellules immunitaires. Elle survient lorsque la croissance rapide des cellules cancéreuses dépasse la capacité du tissu à former de nouveaux vaisseaux sanguins. Certaines régions deviennent alors très pauvres en oxygène, ce qui perturbe profondément le fonctionnement du système immunitaire et limite l’efficacité de nombreuses immunothérapies.
Parmi les cellules les plus affectées par ce manque d’oxygène figurent les cellules dendritiques. Ces sentinelles du système immunitaire détectent les antigènes tumoraux et activent les lymphocytes T responsables de la destruction des cellules cancéreuses. Dans un environnement hypoxique, leur capacité à capter les antigènes, migrer vers les ganglions lymphatiques et déclencher une réponse immunitaire efficace est fortement altérée. De plus, elles ne sont pas seulement immunosupprimées : elles peuvent également acquérir un phénotype tolérigène et protumoral, contribuant ainsi à l’échappement immunitaire. Les cellules cancéreuses s’adaptent quant à elles facilement à ce manque d’oxygène et ne sont donc pas fragilisées par ce phénomène qui est à la fois une conséquence de la croissance rapide de la tumeur et un bouclier qu'elle exploite, notamment pour neutraliser les cellules immunitaires.
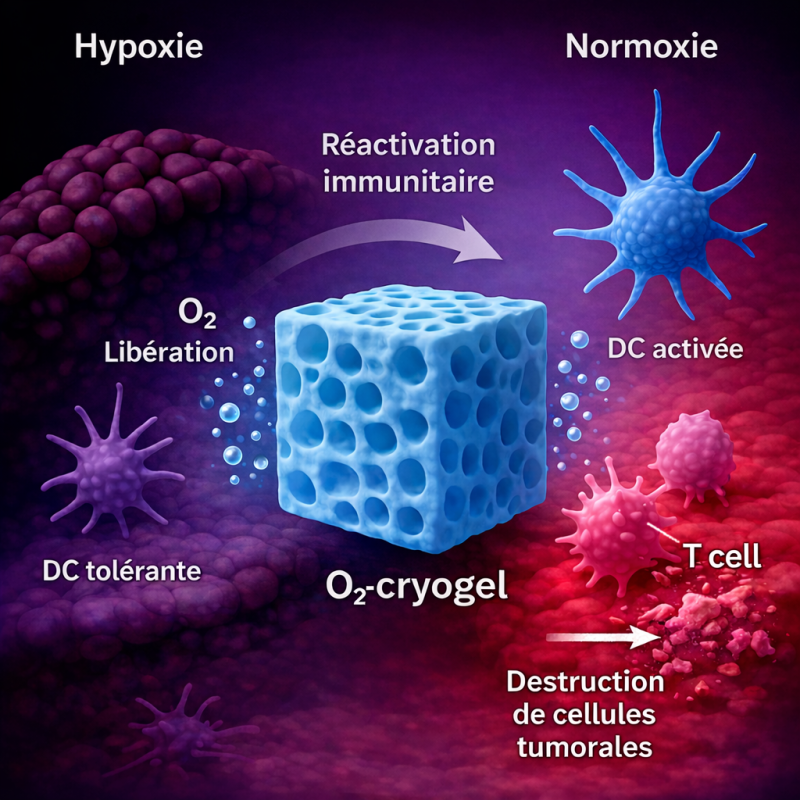
Pour contrer ce phénomène, une équipe franco-américaine du laboratoire Polymères, biopolymères, surfaces (CNRS/Université de Rouen Normandie) et de la Northeastern University (Boston), a mis au point des biomatériaux polymères injectables appelés O₂-cryogels. Ces structures macroporeuses, composées notamment d’acide hyaluronique, sont comparables à des éponges souples et élastiques chargées en peroxyde de calcium (CaO2). Hautement déformables et compressibles, elles peuvent être directement injectées à la seringue dans les tissus tumoraux de manière non invasive. Elles y retrouvent leur forme après injection et libèrent progressivement de l’oxygène par hydrolyse du peroxyde de calcium au contact de l’eau des tissus.
Cette oxygénation du microenvironnement tumoral permet de restaurer l’activité des cellules immunitaires. Les cellules dendritiques retrouvent leur capacité antitumorale, notamment à capter les antigènes tumoraux, à migrer vers les ganglions et à activer les lymphocytes T. Les lymphocytes T cytotoxiques prolifèrent davantage et la destruction des cellules tumorales est significativement renforcée. En rétablissant un environnement immunitaire actif, cette stratégie pourrait transformer certaines tumeurs dites « froides », peu infiltrées par les cellules immunitaires, en tumeurs « chaudes », plus susceptibles de répondre aux immunothérapies. Au‑delà de cette preuve de concept publiée dans la revue Cell Biomaterials, ces biomatériaux pourraient devenir une plateforme thérapeutique polyvalente pour renforcer l’efficacité de nombreuses stratégies d’immunothérapie existantes, comme les vaccins anticancéreux ou les thérapies cellulaires actuellement en cours d’investigation.
Rédacteur : Anne-Valerie FOILLARD RUZETTE
Référence
Bioengineered cryogels overcome hypoxia-driven tolerance and restore antitumor immunity
Bhatt, K., Colombani, T., Nukovic, A., Parekh, N., Hamrangsekachaee, M., Rogers, Z. J., Sitkovsky, M., Hatfield, S., & Bencherif, S. A.
Cell Biomaterials 2026
https://doi.org/10.1016/j.celbio.2026.100417