Quelle formule est à l’origine de la physique statistique ?
L. Boltzmann et J.W. Gibbs, célèbres physiciens du XIXème siècle, ont chacun proposé une formule pour calculer les paramètres thermodynamiques d’objets macro ou microscopiques, formules qui donnent des résultats différents lorsque le système est constitué de quelques atomes uniquement. Mario Barbatti, professeur à l’Institut de chimie radicalaire de l’Université Aix Marseille (CNRS/ Aix-Marseille université) et l’Institut universitaire de France, propose une théorie qui pourrait permettre de trancher la question et clore le débat vigoureux entre les partisans de chacune de ces formules qui sont à l’origine de la physique statistique.
Sur la tombe de Ludwig Boltzmann, à Vienne, on peut lire en guise d’épitaphe l’équation qui l’a rendu célèbre : S = log W, expression qui relie l’entropie d’une substance (S) au nombre (W) d’états microscopiques de même énergie. Boltzmann a ensuite montré comment toutes les autres quantités thermodynamiques, et en particulier la température, pouvaient être tirées de cette équation, jetant ainsi les fondements de la physique statistique de la fin du XIXe siècle.
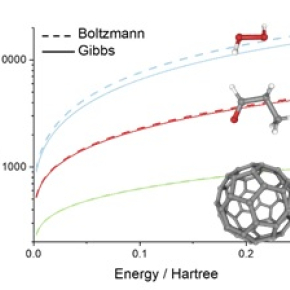
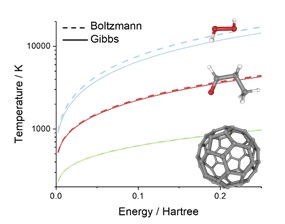
Et c’est là qu’intervient dans le débat scientifique un autre fondateur de la physique statistique, Josiah Willard Gibbs qui, à la même époque, propose que l’entropie soit liée non pas au nombre d’états dans lesquels peut se trouver le système, ayant la même énergie, mais à tous les états accessibles quelle que soit leur énergie. Si les deux formulations donnent effectivement les mêmes paramètres thermodynamiques pour les substances ordinaires, ça n’est plus le cas pour plusieurs matériaux quantiques complexes. Le débat, parfois vigoureux, entre les partisans de la formulation de Boltzmann et celle de Gibbs est lancé et, à ce jour, personne n’a encore pu déterminer expérimentalement laquelle des deux approches était la bonne.
Mario Barbatti, professeur à l’Institut de chimie radicalaire de l’Université Aix Marseille (CNRS/ Aix-Marseille université) et l’Institut universitaire de France, propose une théorie qui pourrait permettre de trancher la question et clore le débat. Il a en effet récemment montré que, pour une très petite molécule isolée (moins de 10 atomes), les températures prédites par les formules de Gibbs et de Boltzmann sont suffisamment différentes pour être mesurées et mettre fin au débat. Même si, dans ce cas, cette mesure par fluorescence peut s’avérer complexe, les physiciens disposent de tous les outils pour la réaliser rapidement. Un résultat qui pourrait s’avérer crucial pour connaître enfin les véritables fondements de la physique statistique qui relie le monde microscopique des transitions quantiques des molécules aux concepts macroscopiques plus courants comme la pression ou la température.
Ces travaux ont été financés par le Conseil européen de la recherche dans le cadre de la subvention ERC advanced grant SubNano (grant agreement 832237).
Rédacteur : CCdM
Référence
Mario Barbatti
Defining the Temperature of an Isolated Molecule
J. Chem. Phys. 156, 204304 (2022)
https://doi.org/10.1063/5.0090205
Versions de ce travail en libre accès :
https://hal.archives-ouvertes.fr/hal-03666814v1