Optimiser la chimiothérapie grâce à des jumeaux numériques
En combinant modélisation et tests in vivo, une équipe de scientifiques est parvenue à entraîner efficacement un modèle de jumeau numérique qui permet de prédire le meilleur protocole d’administration d’un traitement innovant contre le cancer du sein. En modulant les doses et le schéma d’administration grâce à ce modèle, ils ont obtenu une efficacité supérieure aux traitements actuels, jusqu’à 60 % de rémission complète chez la souris sans effets secondaires supplémentaires détectables.
La chimiothérapie reste un pilier du traitement des cancers, mais avec deux défauts majeurs : une efficacité parfois limitée et des effets secondaires importants. À cela s’ajoute une contrainte pratique non négligeable : la plupart des traitements sont administrés par voie intraveineuse, une méthode lourde pour les patients et coûteuse pour les systèmes de santé. Pour contourner ces limites, les scientifiques développent depuis plusieurs années des « nanomédicaments », capables de mieux cibler les tumeurs et de circuler plus longtemps dans l’organisme. Ils étudient également leur administration par la voie sous-cutanée, qui est plus confortable pour le patient et moins coûteuse que la voie intraveineuse. Mais plusieurs défis persistent, et notamment celui d’optimiser les protocoles d’administration de ces traitement innovants sans multiplier les tests sur les animaux.
C’est précisément la question abordée par une équipe interdisciplinaire de chimistes de l’Institut Gallien Paris-Saclay (CNRS/Université Paris-Saclay) et de biologistes et mathématiciens du Centre de recherche en cancérologie de Marseille (Inria/Inserm/CNRS/Aix-Marseille Université/Institut Paoli Calmettes). Les scientifiques ont conçu un modèle combinant pharmacocinétique (le devenir du médicament dans l’organisme) et pharmacodynamique (son effet sur la tumeur) qui leur permet de prédire l’efficacité d’un traitement thérapeutique en fonction des dosages et de la durée et séquence du traitement. Ils ont appliqué ce modèle à un anticancéreux innovant : une version modifiée du paclitaxel, largement utilisé en chimiothérapie, qui est ici lié à un polymère hydrosoluble pour permettre son injection par voie sous-cutanée. Cette molécule, appelée prodrogue polymère, permet une libération lente du médicament et pourrait, à terme, faciliter des traitements à domicile ou dans des zones géographiques éloignées de centres hospitaliers.
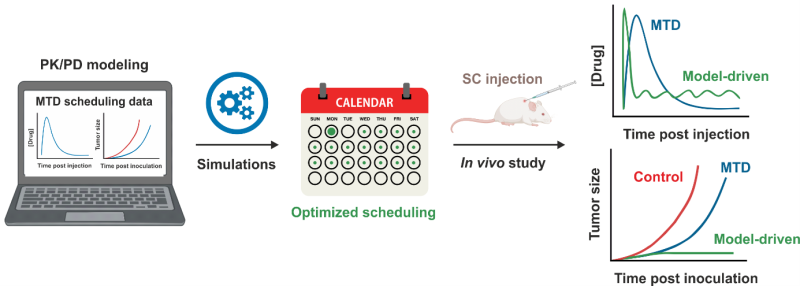
Pour développer ce modèle, l’équipe a mis en œuvre une approche intégrative in vivo / in silico (simulation). Un ensemble de données expérimentales initial disponible pour la prodrogue polymère a été utilisé pour établir et entraîner le modèle. Ses capacités prédictives ont été vérifiées sur un schéma d’administration distinct de l'ensemble de données d'apprentissage et testé in vivo. L’efficacité de dizaines de schémas thérapeutiques différents a ensuite pu être évaluée in silico sans avoir à les tester sur des souris, rendant ainsi la démarche plus éthique.
Ces prédictions suggèrent que les protocoles classiques, basés sur l’administration espacée des doses maximales, ne sont pas les plus efficaces pour cette prodrogue polymère. En revanche, une forte dose initiale suivie d’injections quotidiennes de faibles doses permet de mieux contrôler la tumeur. Cette stratégie tient compte du fait que la tumeur devient moins sensible au traitement après la première administration, signe qu’une résistance s’installe rapidement ou que les cellules les moins résistantes meurent initialement. Les prédictions ont ensuite été testées sur des souris porteuses de tumeurs, ce qui a permis de démontrer : (i) une très bonne adéquation entre les prédictions et les résultats expérimentaux et (ii) que le schéma optimal identifié par le modèle conduit à une régression tumorale durable et jusqu’à 60 % de rémission complète, sans effets secondaires supplémentaires détectables.
Cette étude, publiée dans la revue Advanced Healthcare Materials, ouvre des perspectives importantes au-delà de la preuve de concept. Elle suggère que les modèles numériques pourraient devenir des outils clés pour optimiser des traitements innovants à base de nanomédicaments en réduisant les coûts et le recours aux expérimentations animales. À terme, ces « jumeaux numériques » pourraient même être adaptés à chaque patient, pour personnaliser les doses et le rythme d’administration et maximiser l’efficacité des thérapies tout en limitant leurs effets indésirables.
Rédacteur : AVR
Référence
Model-Driven Optimization of Subcutaneous Polymer Prodrugs Achieves Cancer Remission in Mice
Anne Rodallec, Randy Lee, Jingming Cao, Sophie Marolleau, Julien Nicolas & Sébastien Benzekry
Advanced Healthcare Materials 2026
https://doi.org/10.1002/adhm.202505872