Observer les récepteurs de l’inflammation au nanomètre près grâce à la chimie
Des scientifiques du CNRS sont parvenus à marquer et observer finement les récepteurs qui contrôlent le déclenchement de l’inflammation et leur organisation spatiale en fonction de la réaction. Une étape clé pour avancer dans le traitement de la douleur et de maladies inflammatoires, à retrouver dans la revue eLife.
La réaction inflammatoire est indispensable au vivant pour se défendre et réparer les tissus. Lorsqu’une infection ou une lésion survient, les cellules immunitaires du système nerveux central, les microglies, s’activent pour déclencher et contrôler cette réaction. Elles détectent des signaux de danger, comme l’ATP libéré par les cellules endommagées, ce qui entraîne la production de molécules pro-inflammatoires. Cette détection se fait grâce à des récepteurs spécifiques exprimés par les microglies, par exemple le récepteur P2X7. Le rôle clé de ce récepteur dans le déclenchement et le contrôle de l’inflammation en fait d’ailleurs une cible thérapeutique potentielle pour les maladies inflammatoires. Cependant, la manière dont ces récepteurs sont exprimés et s’organisent à la surface des microglies pendant l’inflammation reste mal connue.
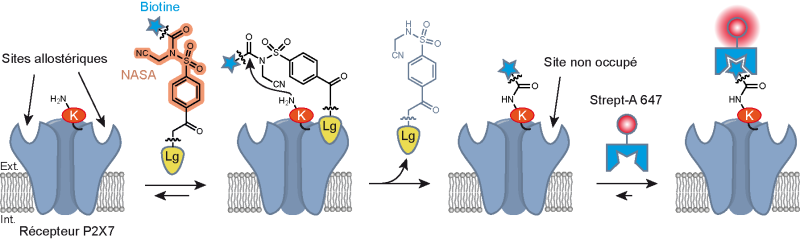
Des chimistes et biologistes1 du CNRS, de l’Université de Strasbourg et de l’Université de Bordeaux ont développé une nouvelle méthode chimique permettant de marquer de façon spécifique et observer directement par imagerie à très haute résolution les récepteurs P2X7 exprimés par une lignée de microglie de souris faciles à cultiver in vitro. Ce marquage en deux étapes repose d’abord sur l’introduction sélective de molécules de biotine sur des résidus lysine des récepteurs P2X7. Pour cette étape, les scientifiques ont synthétisé un réactif constitué de trois éléments : un ligand hautement sélectif du récepteur P2X7 à l’une de ses extrémités, une molécule de biotine à l’autre, et un centre électrophile réactif vis-à-vis des résidus lysine. Cette architecture permet de cibler sélectivement les récepteurs P2X7 et y accrocher efficacement la biotine sur les résidus lysine localisés à proximité du site du ligand. Un marqueur fluorescent peut ensuite facilement être accroché de manière sélective à la biotine pour faire de l’imagerie à très haute résolution (microscope dSTORM).
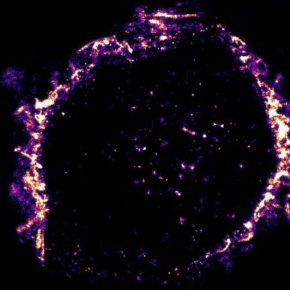
L’équipe a ainsi pu visualiser pour la première fois l’organisation des récepteurs P2X7 à l’échelle nanométrique. Les résultats montrent que les récepteurs P2X7 exprimés dans la membrane des microglies, initialement isolés, se réorganisent en amas lors du déclenchement d’une réponse inflammatoire. Ces amas participent ensuite à la libération massive des molécules pro-inflammatoires. Cette découverte suggère d’ailleurs que cibler l’organisation fine des récepteurs P2X7 et la contrôler pourrait ouvrir de nouvelles stratégies thérapeutiques visant à contrôler l’inflammation. Ce nouvel outil de chémo-biologie vient renforcer l’arsenal avec lequel le monde du vivant peut être sondé à l’échelle nanométrique pour mieux le comprendre et le soigner. Ces résultats sont parus dans la revue eLife.
Rédacteur : AVR
- 1Du laboratoire de Chémo-biologie synthétique et thérapeutique (CNRS/Université de Strasbourg), de l’Institut interdisciplinaire de neurosciences (CNRS/Université de Bordeaux) et de l’Institut des neurosciences cellulaires et intégratives (CNRS)
Référence
Affinity-guided labeling reveals P2X7 nanoscale membrane redistribution during BV2 microglial activation
Benoit Arnould, Adeline Martz, Pauline Belzanne, Francisco Andrés Peralta, Federico Cevoli, Volodya Hovhannisyan, Yannick Goumon, Eric Hosy, Alexandre Specht & Thomas Grutter
eLife 2026
https://doi.org/10.7554/eLife.106096.3