Cibler un ARN oncogène par des petites molécules durables et efficaces
Dans un article paru dans la revue Chemistry A European Journal, des scientifiques dévoilent une bibliothèque de petites molécules qui ciblent un ARN bien connu pour favoriser le développement de certaines tumeurs. La méthode de synthèse en cinq étapes des molécules de ciblage, qui respecte les principes de la chimie verte, et leur activité inhibitrice prometteuse ouvrent de nouvelles perspectives dans le traitement de certains cancers
Cibler l’ARN pour soigner des pathologies infectieuses ou cancéreuses ou encore des maladies inflammatoires ou rares est une stratégie thérapeutique en plein essor. En particulier, la conception de petites molécules, appelées ligands, capables d'interagir en se liant de manière sélective à une cible ARN choisie représente un défi majeur pour la chimie médicinale. En effet, la plupart des médicaments connus ciblent des protéines, qui ne représentent qu’une très petite partie de ce que le génome humain produit. La majeure partie de cette production consiste en une myriade d’ARNs qui sont impliqués dans de très nombreuses fonctions biologiques comme le transport de l’information génétique, la synthèse des protéines, la régulation de l’expression des gènes ou le métabolisme cellulaire.
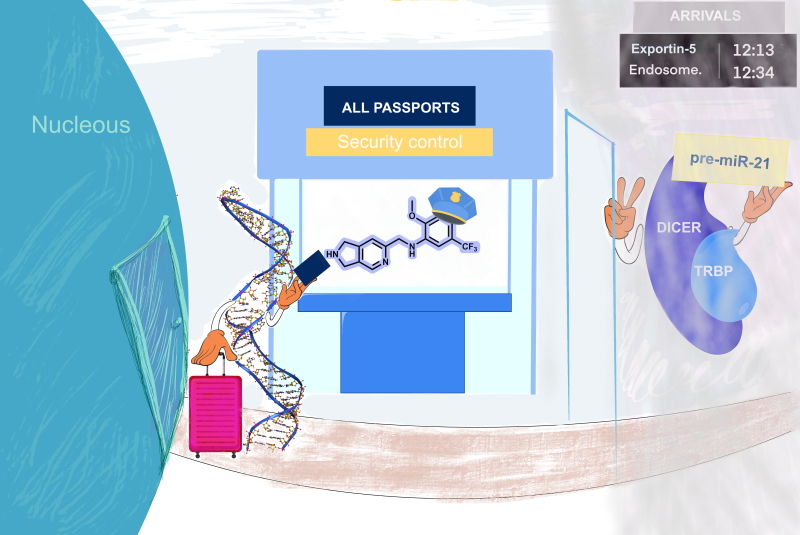
C’est dans ce contexte que des équipes de l’Institut de chimie de Nice (CNRS/Université Côte d’Azur) et du IQS School of Engineering Universitat Ramon Llull de Barcelone ont élaboré toute une famille de ligands d'ARN à partir d'une brique de base unique : un noyau aromatique de type pyridine fonctionnalisée. En modifiant cette brique de base, ils ont conçu et synthétisé toute une bibliothèque de petites molécules qui ciblent la production du micro-ARN 21 (miR-21). Ce micro-ARN impliqué dans de très nombreux processus physiologiques et pathologiques régule notamment la prolifération des cellules cancéreuses.
La stratégie de synthèse de cette famille de ligands est basée sur une étape clé de catalyse au ruthénium, selon un processus de cyclisation à économie d’atome qui respecte au mieux les 12 principes de Chimie Verte. En utilisant cette approche durable, les molécules ont été conçues pour se lier spécifiquement à la structure en épingle à cheveux du pré-miR-21 et inhiber ainsi le fonctionnement de l’enzyme responsable de la maturation du miR-21.
L’étude montre que les molécules sélectionnées ont une très grande affinité pour le pré-miR-21 et une bonne sélectivité contre d'autres structures d'acides nucléiques. L’étude de leur mécanisme d'action a permis d'identifier les parties des composés les plus actives et d'établir des relations structure-activité inédites. Ces résultats, à retrouver dans la revue Chemistry – A European Journal, ouvrent la voie à de nouvelles stratégies durables pour cibler les microARN oncogènes ou leur production.
Référence
De-Novo Design of pre-miR-21 Maturation Inhibitors: Synthesis and Activity Assessment
Iryna Shcheholeva, Daniel Fernández-Remacha, Roger Estrada-Tejedor, Maria Duca et Véronique Michelet
Chem. Eur. J. 2023
https://doi.org/10.1002/chem.202300825