Catalyse organique : de l’utilité des carbènes dans la chimie du Bore
Construire des molécules organiques d’intérêt dotées de propriétés particulières, thérapeutiques, olfactives, optiques, électriques…est tout l’art de la chimie de synthèse. Dans la plupart des cas, cela nécessite l’utilisation de catalyseurs, ces molécules qui activent certaines liaisons et favorisent une réaction chimique particulière sans être incorporés au produit final. Si la catalyse a longtemps été le domaine des enzymes, dans la nature, et des métaux de transition, en chimie de synthèse, le paysage a drastiquement évolué avec le Prix Nobel de Chimie attribué en 2021 à Benjamin List et David MacMillan pour leurs travaux sur la catalyse organique. De tels catalyseurs permettent en effet des procédés de chimie plus verte et qui évitent les problèmes de purification finale des produits formés, deux gros inconvénient des catalyseurs à base de métaux de transition traditionnellement utilisés.
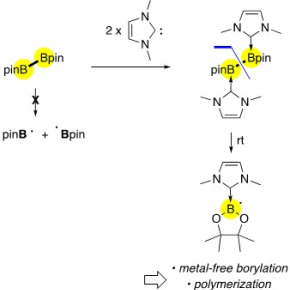
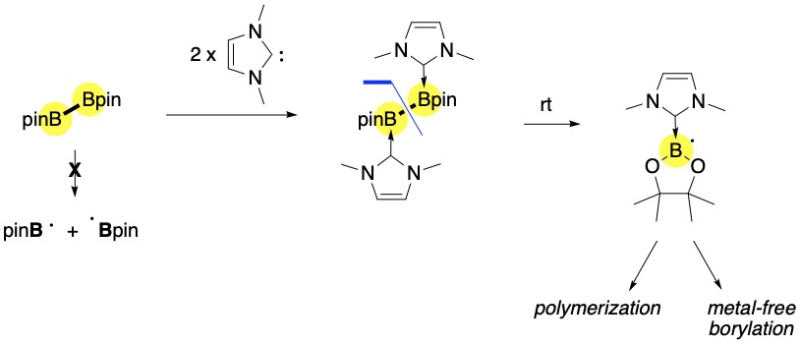
Les molécules organiques qui comportent une liaison Bore-Bore (B-B) font partie des briques de base très utilisées en chimie de synthèse. Cette liaison est en effet aisément activable par de nombreux procédés catalytiques qui permettent d’installer le B sur de nombreuses molécules et matériaux fonctionnels. Des chimistes français ont récemment étudié les mécanismes d’activation de cette liaison dans une molécule commerciale, le bis(pinacolato)diborane, par une base de Lewis organique de la famille des carbènes.* Ils montrent, par une combinaison de techniques d’analyse chimique et de calculs théoriques, que les espèces intermédiaires de ce procédé catalytique sont des radicaux, qui ouvrent la voie à de nombreuses réactions de chimie organique, la polymérisation notamment. En jouant sur la structure et le nombre carbènes utilisés, ils ont en effet pu développer des molécules dont la stabilité peut être aisément régulée, qu’il s’agisse de l’augmenter pour pouvoir observer et comprendre les schémas réactionnels intermédiaires lors de l’activation de ces molécules, ou au contraire la diminuer pour former des molécules activables à température et pression ambiante, mais qui ne présentent pour autant aucun danger de stockage. Ces résultats, à retrouver dans la revue Chemical Science, apportent un éclairage nouveau sur la catalyse organique des molécules borylées et les mécanismes radicalaires associés.
* Les carbènes sont des espèces chimiques à base de carbone possédant seulement 6 électrons de valence, ce qui les rend ultra-réactifs.
Rédacteur: AVR
Référence
NHC induced radical formation via homolytic cleavage of B–B bonds and its role in organic reactions.
Laura Kuehn, Ludwig Zapf, Luis Werner, Martin Stang, Sabrina Würtemberger-Pietsch, Ivo Krummenacher, Holger Braunschweig, Emmanuel Lacôte*, Todd B. Marder* et Udo Radius*, Chemical Science, 7 juin 2022.