Cancer et chimiothérapie ciblée : trois questions à Alexandre Detappe et Vincent Mittelheisser
Traiter les cancers par une chimiothérapie qui cible uniquement les tumeurs en limitant voire supprimant les effets secondaires sur les tissus sains, voilà le graal que cherchent à atteindre la chimie thérapeutique et la médecine. Alexandre Detappe, chercheur à l’Institut pluridisciplinaire Hubert Curien du CNRS et à l’Institut de Cancérologie de Strasbourg Europe (ICANS), ainsi que Vincent Mittelheisser, étudiant en thèse à l’ICANS, nous présentent les solutions les plus prometteuses et les verrous qui restent à lever pour que de telles thérapies voient le jour.
La chimiothérapie sans effets secondaires, une promesse tenue ?
Améliorer l’efficacité des chimiothérapies passe en effet par la mise au point de stratégies de ciblage spécifique des cellules tumorales qui permettent d’administrer de façon plus efficace une quantité moindre de médicaments et de limiter autant que possible les effets toxiques sur les tissus sains. Deux voies sont activement étudiées pour atteindre ce but et vectoriser, c’est-à-dire transporter, les molécules thérapeutiques uniquement là où on souhaite qu’elles agissent : les conjugués anticorps-médicaments (ADCs) et les nanoparticules (NPs) chargées de médicament.
Déjà utilisée dans les traitements de routine des hémopathies malignes ou des cancers du sein, la première voie permet un ciblage tumoral élevé grâce à une reconnaissance chimique par des anticorps monoclonaux synthétisés précisément pour reconnaître les cellules de la pathologie ciblée. Le nombre moyen de molécules médicaments que chaque anticorps peut véhiculer tout en restant spécifique est cependant très limité. Les NPs peuvent quant à elles contenir de très nombreuses molécules thérapeutiques et s’accumulent passivement dans les tumeurs. Cependant, ce ciblage passif limite la dose de NPs atteignant la tumeur et ne permet pas de contrôler où celles-ci s’accumulent, parfois de manière très hétérogène au sein d’une tumeur.
Il semble donc naturel de chercher à combiner la sélectivité de ciblage des anticorps à la capacité d’encapsulation et/ou de conjugaison des NPs.
Plus de 160 publications passées au crible, quels sont les résultats les plus prometteurs ?
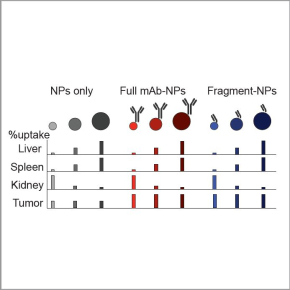
Dans une perspective publiée dans Advanced Materials, et basée sur une vaste étude* des travaux parus au cours de 12 dernière années, nous avons identifié les paramètres physicochimiques optimaux pour 3 types de nanoparticules (inorganiques/organiques, polymériques et lipidiques) conjuguées à des anticorps monoclonaux ou à des fragments d’anticorps. Nous avons ainsi déterminé les couples qui permettent d’obtenir le meilleur ciblage tumoral : les NPs inorganiques/organiques et polymériques ciblées par des anticorps monoclonaux et les NPs lipidiques ciblées par des fragments d’anticorps. Cette étude montre que les paramètres pharmacocinétique et de biodistribution sont dictés par les NPs, indépendamment de l’utilisation d’anticorps monoclonaux ou de fragments d’anticorps. Elle confirme donc l’importance d’optimiser la conception des NPs pour améliorer la délivrance à la tumeur.
Quels obstacles doivent encore être surmontés pour proposer de telles thérapies aux patients ?
Si les résultats précliniques et les premières phases d’essais cliniques sur un nombre restreint de patients semblent valider l'intérêt d'utiliser des NP combinées à des anticorps, le rapport coût/efficacité reste encore à déterminer. Seule une étude beaucoup plus vaste et contrôlée de l’efficacité réelle de cette stratégie, qui compare et analyse de façon statistique l’efficacité thérapeutique observée pour un grand nombre de patients à celle obtenue pour des tests de contrôle avec une molécule classique, pourra en effet déterminer si le coût (production d'anticorps, synthèse de NPs, conjugaison, et reproductibilité) est justifié par une amélioration notable et reproductible. Reste à espérer que les recherches très actives dans le domaine au niveau mondial permettront de lever ce verrou.
*Etude financée en partie par le Conseil européen de la recherche, bourse ERC Starting TheranoImmuno, grant agreement No. 95010.
Rédacteur: AVR
Référence
Optimal physicochemical properties of antibody-nanoparticle conjugates for improved tumor targeting
V. Mittelheisser, P. Coliat, E. Moeglin, L. Goepp, J.G. Goetz, L.J. Charbonnière, X. Pivot et A. Detappe Advanced Materials 2022