Alzheimer : de nouveaux agents de contraste
Un consortium de chercheurs européens mené par plusieurs laboratoires lyonnais propose un nouvel agent d'imagerie « multi-techniques » (IRM, RX, fluorescence…) ciblant les plaques amyloïdes-β (Aβ), premiers signes pathologiques de la maladie d'Alzheimer (MA). Ces résultats sont parus dans la revue Nanomedecine.
Les plaques amyloïdes Aβ, agrégats de protéines qui envahissent progressivement le cerveau, participent à la dégradation des communications entre les neurones. Premiers signes pathologiques de la maladie d'Alzheimer, elles apparaissent silencieusement dans le cerveau des décennies avant que les symptômes de la maladie ne se manifestent. Pour les détecter dans le cerveau, la seule solution à ce jour est d’avoir recours à des techniques de médecine nucléaire (imagerie à l’aide d’un traceur radioactif).
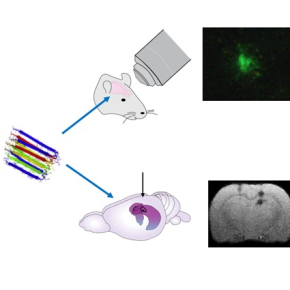
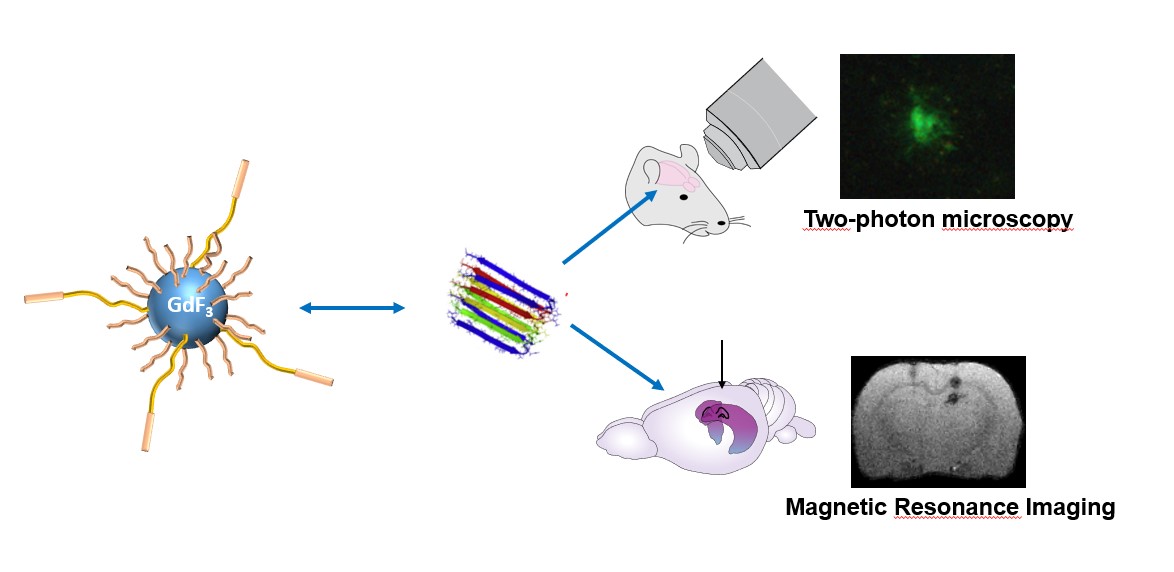
Un consortium européen, mené par des scientifiques du Laboratoire de chimie (CNRS/ENS de Lyon/Université Claude Bernard Lyon 1) et du Centre de recherche en neurosciences de Lyon (CNRS/Université Claude Bernard Lyon 1/Université de St Etienne/Inserm), ont conçu, caractérisé et évalué sur différents modèles animaux, un nouvel agent d'imagerie multimodal ciblant les plaques amyloïdes-β (Aβ). L’originalité de cet agent de contraste : sous forme de nanoparticules de fluorure de gadolinium, il est enrobé d'une molécule spécifiquement conçue pour se lier aux plaques Aβ. Le noyau gadolinium, facilement observable en imagerie par résonance magnétique (IRM) mais aussi par imagerie aux rayons X, et la molécule greffée, détectable en imagerie par fluorescence, permettent ainsi de croiser plusieurs types d'imagerie pour étudier la pathologie à différentes échelles spatiales et mieux la diagnostiquer.
Dans ce travail publié dans la revue Nanomedecine, la stabilité et les propriétés magnétiques et fluorescentes de l'agent de contraste ont été vérifiées in vitro (en tubes). La capacité de l'agent de contraste à se lier aux plaques Aβ et à fournir un signal détectable en IRM, rayons X ou imagerie de fluorescence, a ensuite pu être démontrée in vivo dans des modèles rongeurs (rats et souris présentant des plaques amyloïdes Aβ). Des résultats qui montrent que cette nouvelle classe d'agents de contraste polyvalents pourra maintenant être utilisée pour cibler des processus pathologiques dans le cerveau.
Rédacteur : CCdM
Référence
Frédéric Lerouge, Elodie Ong, Hugo Rositi, Francis MPambani, Lise-Prune Berner, Radu Bolbos, Cécile Olivier, Françoise Peyrin, Vinu Apputukan, Cyrille Monnereau, Chantal Andraud, Frederic Chaput, Yves Berthezène, Bettina Braun, Mathias Jucker, Andreas K.O. Åslund, Sofie Nyström, Per Hammarström, K. Peter R. Nilsson, Mikael Lindgren, Marlène Wiart, Fabien Chauveau & Stephane Parola
In vivo targeting and multimodal imaging of cerebral Aβ-amyloid aggregates using hybrid GdF3 nanoparticles
Nanomedecine 2023
https://www.futuremedicine.com/doi/10.2217/nnm-2022-0252