Les nanoparticules d’or en milieu biologique moins inertes qu’on ne le pensait
Les scientifiques de l'Institut de chimie physique (CNRS/Université Paris-Saclay) ont montré que les nanoparticules d’or, utilisées pour le diagnostic médical ou plus récemment comme agents thérapeutiques, présentaient une activité catalytique insoupçonnée qui pourrait rendre intelligibles de nombreux résultats expérimentaux restés jusqu'à présent inexpliqués.
L’utilisation des nanoparticules d'or (AuNP) dans divers domaines des sciences de la santé ne fait qu’augmenter. On les utilise pour l’imagerie et pour le diagnostic mais aussi, après fonctionnalisation de leur surface, pour transporter des substances actives comme des médicaments vers des cibles (organes, cellules...). Cet engouement pour l’or est souvent justifié par l'absence d'activité chimique, donc de toxicité, des AuNP vis-à-vis du milieu biologique… Il semblerait qu’il n’en soit rien !
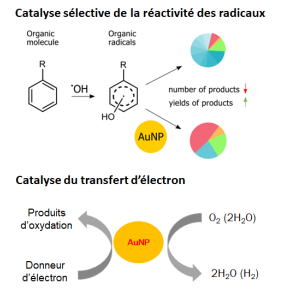
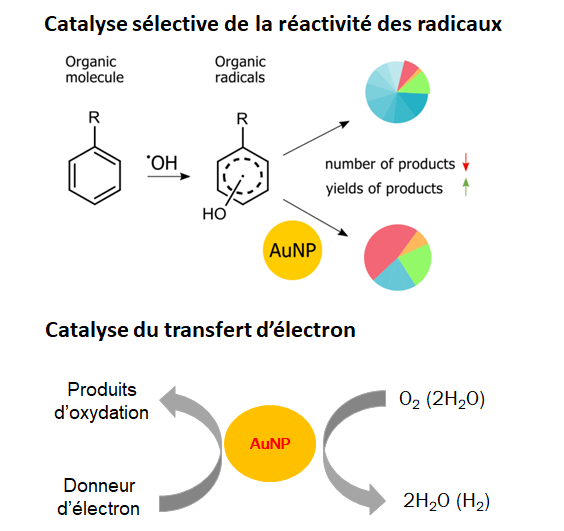
En effet, les scientifiques de l'Institut de chimie physique (CNRS/Université Paris-Saclay) montrent que ces nanoparticules brutes, non fonctionnalisées, ne sont pas chimiquement neutres et se révèlent même d’excellents catalyseurs pouvant modifier les schémas réactionnels habituels. Prenons le cas de la réaction d’hydroxylation de l'acétanilide en présence d’O2. L’acétanilide est en effet le précurseur de nombreuses molécules organiques comme la pénicilline, le paracétamol ou le camphre, et son hydroxylation est étudiée comme modèle de monooxygénase du cytochrome P-450. Les scientifiques constatent que l’ajout de nanoparticules d’or provoque une diminution d’un facteur 40 de la formation du produit de réaction. Observation inattendue car, en l'absence de nanoparticules d'or, l'oxygène est connu pour favoriser les réactions d'hydroxylation. Par contre, l’oxydation de la vitamine C, qui est un donneur d'électrons, est accélérée plus de 1000 fois en présence d'AuNPs. Plus généralement, les NP d'or en présence d'O2 favorisent l’oxydation des espèces donneuses d'électrons comme les radicaux ou certaines molécules présentes dans le milieu biologique.
On peut par conséquent s'attendre à ce que les AuNPs puissent également altérer le métabolisme cellulaire en oxydant les radicaux organiques naturellement produits dans la cellule ou en oxydant les molécules donneuses d’électrons présentes dans son environnement. Cette activité catalytique à température ambiante jusqu’à maintenant ignorée lors de l’introduction des AuNPs dans les milieux biologiques devra maintenant être prise en compte pour comprendre les mécanismes réactionnels mis en jeu et, pourquoi pas, rendre intelligibles de nombreux résultats expérimentaux restés jusqu'à présent inexpliqués.
(*) L’acétanilide est le précurseur de nombreuses molécules organiques comme la pénicilline, le paracétamol ou le camphre. L’hydroxylation de l'acétanilide est étudiée comme modèle de monooxygénase du cytochrome P-450.
Rédacteur : CCdM
Références
Viacheslav Shcherbakov; Sergey A. Denisov & Mehran Mostafavi
On the Primary Water Radicals’ Production in the Presence of Gold Nanoparticles: Electron Pulse Radiolysis Study
Nanomaterials 2020
Shcherbakov, V.; Denisov, S. A.; &Mostafavi, M
Mechanism of organic radicals' oxidation catalysed by gold nanoparticles.
Phys. Chem. Chem. Phys. 2021
Viacheslav Shcherbakov, Sergey A. Denisov & Mehran Mostafavi
A mechanistic study of gold nanoparticles catalysis of O2 reduction by ascorbate and hydroethidine, investigating reactive oxygen species reactivity
RSC Adv. 2023
https://pubs.rsc.org/en/content/articlelanding/2023/ra/d3ra00443k