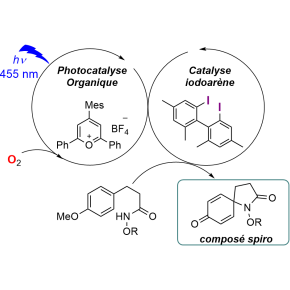
Chimie verte : deux catalyseurs agissent en synergie pour exploiter l’oxygène et la lumière
Idéalement pour l’environnement, les réactions chimiques se dérouleraient avec un nombre réduit de réactifs, à l’aide de catalyseurs, à l’air libre et sous lumière naturelle. Des chercheurs du laboratoire i-CLeHS (CNRS/Chimie ParisTech) et de l’ICSN (CNRS) s’en sont rapprochés en modifiant des molécules organiques grâce à deux catalyseurs, du dioxygène et une lumière bleue. Ces travaux, publiés dans la revue Angewandte Chemie International Edition, proposent ainsi une manière originale, et verte, de synthétiser des molécules particulières appelées bicycles spiraniques, qui sont notamment utilisées en pharmacie et en agrochimie.
Pour suivre les principes de la chimie verte, il est important de produire moins de déchets et de consommer moins d’énergie. Ceci conduit à privilégier les réactions employant des catalyseurs et, si possible, des modes d’activation alternatifs. Pour une réaction d’oxydation, le cas idéal serait par exemple que l’énergie provienne de la lumière naturelle et que l’oxydant soit le dioxygène de l’air. Dans cette perspective, des chercheurs de l’Institut de chimie des substances naturelles (ICSN, CNRS) et de l’Institute of chemistry for life and health sciences (i-CLeHS, CNRS/Chimie ParisTech) ont développé un nouveau système doublement catalytique, capable d’utiliser du dioxygène et de la lumière bleue pour produire des molécules formées de deux cycles organiques, pouvant être différents, via l’oxydation de petites molécules appelées amides. Ces composés bicycles spiraniques, c’est-à-dire reliés par un unique atome plutôt que deux ou plus, de ce type sont utilisés par les industries pharmaceutiques, comme l’antihypertenseur irbésartan, et agrochimiques, l’insecticide spirotetramat par exemple.
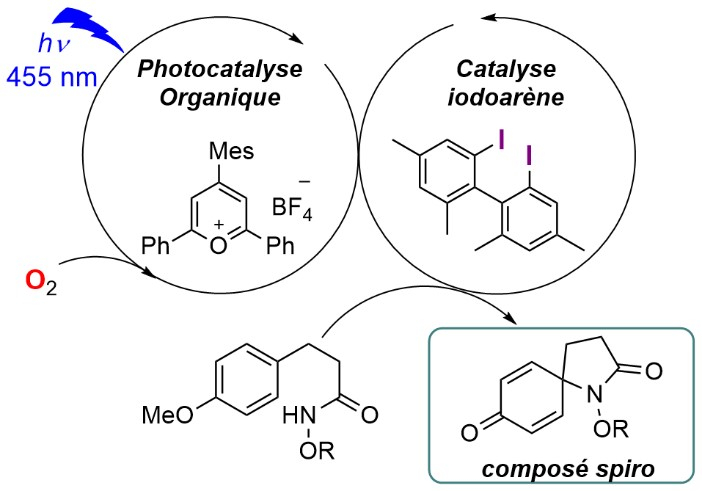
Plus concrètement, les scientifiques ont employé deux molécules organiques simples comme catalyseurs : un sel de pyrylium et un iodoarène. Le premier est activé par une lumière bleue, fournie par un simple ruban de LED disponible dans le commerce, et enclenche l’oxydation de l’iodoarène. On obtient alors un nouveau catalyseur purement organique, qui permet de transformer les amides en plus d’une douzaine de bicycles spiraniques différents. En réagissant avec le dioxygène, le photocatalyseur pyrylium revient ensuite à son état originel. Faciles à obtenir et aisément modulables, ces catalyseurs purement organiques offrent une alternative verte aux systèmes à base de métaux de transition largement utilisés malgré leur rareté, leur prix et leur impact écologique. Les chercheurs espèrent à présent étendre cette stratégie à de nouvelles réactions, notamment asymétriques, afin d’accéder à des molécules plus courantes. Ces travaux ont été financés dans le cadre de l’appel à projets Émergence de l’Institut de Chimie du CNRS (Emergence@INC2019), ce qui a permis un recrutement et l’achat des réactifs et du matériel nécessaire au projet.
Référence
Loïc Habert et Kevin Cariou. Photoinduced aerobic iodoarene‐catalyzed spirocyclization of n‐oxy‐amides to n‐fused spirolactams. Angew. Chem. Int. Ed., 21 septembre 2020.