Contre l’antibiorésistance, une synthèse totale de la tiacumicine B
Alors que les bactéries résistent de mieux en mieux aux antibiotiques, la tiacumicine B cible les pathogènes d’une manière différente de la majorité des antibiotiques. Elle les empêche en effet de fonctionner en bloquant leur production de protéines. Des chercheurs du CNRS, des universités de Paris et de Paris-Saclay en proposent une synthèse totale, avec des nouvelles stratégies et méthodes. Publiés dans la revue Angewandte Chemie International Edition, ces travaux ouvrent la voie à la découverte d’analogues encore plus efficaces.
Problème grave et récurrent, la résistance aux antibiotiques nous laisse de plus en plus vulnérables face aux maladies infectieuses. Afin d’y faire face, de nouveaux modes d’actions et cibles biologiques doivent être identifiés. La tiacumicine B, aussi appelée fidaxomicine, tue ainsi les bactéries en visant leur ARN polymérase, ce qui bloque leur synthèse de protéines sans qu’une résistance n’ait encore été observée. Cette molécule est particulièrement efficace contre Clostridium difficile, une bactérie qui cause une infection nosocomiale intestinale et mortelle. La tiacumicine B a reçu une autorisation accélérée de mise sur le marché aux États-Unis dès 2011, et est actuellement obtenue par fermentation d’actinobactéries. Des chercheurs de l’Institut de chimie des substances naturelles (ICSN, CNRS), du laboratoire Cibles thérapeutiques et conception de médicaments (CiTCoM, CNRS/Université de Paris) et de l’Institut de chimie moléculaire et des matériaux d’Orsay (ICMMO, CNRS/Université Paris-Saclay) viennent de proposer une synthèse totale de la tiacumicine B, c’est à dire en partant uniquement de réactifs organiques simples.
Une autre synthèse totale avait déjà été réalisée par une équipe Suisse, mais cette nouvelle voie est beaucoup plus efficace lors des étapes critiques de glycosylation. Deux sucres rares doivent en effet être attachés au cœur de la molécule avec une liaison spécifique, ce que cette synthèse parvient à réaliser efficacement. Elle gère également mieux les groupements protecteurs, chargés de masquer puis relibérer des fonctions chimiques à des moments précis du schéma de synthèse. Cette méthode permettra d’obtenir des molécules analogues, les chercheurs espérant ainsi trouver des composés encore plus efficaces contre les infections nosocomiales et étudier leur mécanisme d’action biologique.
Référence :
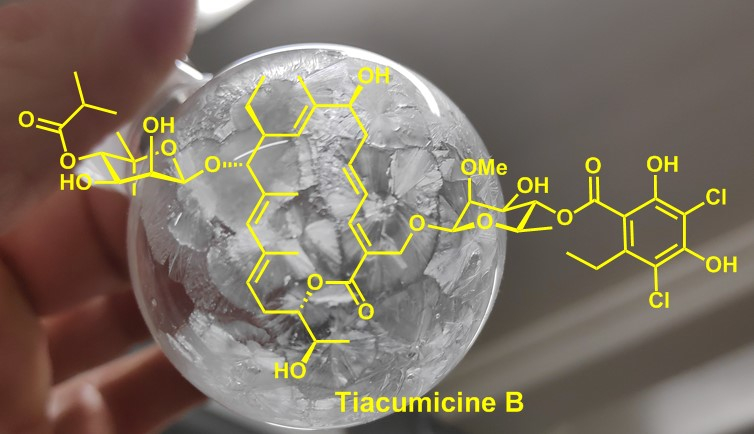
Stéphanie Norsikian, Cedric Tresse, Marc François-Eude, Louis Jeanne-Julien, Guillaume Masson, Vincent Servajean, Grégory Genta-Jouve, Jean-Marie Beau, and Emmanuel Roulland. Total Synthesis of Tiacumicin B: Implementing H-bond-Directed Acceptor Delivery for Highly Selective b-Glycosylations. Angewandte Chemie International Edition.
